Importation de BESREMi (ropeginterféron alfa-2b-njft) en solution injectable, autorisé aux États-Unis, en raison de la pénurie actuelle de PEGASYS (peginterféron alfa-2a) en solution injectable, autorisé au Canada
Résumé
Voir les messages clés ci-dessous
Produits visés
Nom du produit |
Forme pharmaceutique, concentration et format d’emballage |
Pays d’autorisation et code d’identification |
Fabricant |
Importateur au Canada |
|---|---|---|---|---|
BESREMi (ropeginterféron alfa-2b-njft) solution injectable |
Injection : solution à 500 mcg/mL en seringue préremplie unidose, pour usage sous-cutané (sans conservateur). |
États-Unis NDC : 73536-500-01 |
PharmaEssentia Corporation |
Innomar Strategies Inc. pour le compte de FORUS Therapeutics Inc. |
Problème
Il y a une grave pénurie de PEGASYS (peginterféron alfa-2a) en solution injectable en raison de perturbations dans la production. Cette pénurie présente des risques graves aux patients canadiens qui dépendent d’une thérapie à base d’interféron pour le traitement des néoplasmes myéloprolifératifs (NMP). Bien que PEGASYS ne soit pas autorisé par Santé Canada pour cet usage, il a été prescrit hors indication pour traiter cette maladie. Face à ce besoin médical critique, Santé Canada a autorisé FORUS Therapeutics Inc. à importer et à vendre, à titre exceptionnel et temporaire, un produit similaire, mais non identique, le BESREMi (ropeginterféron alfa-2b-njft) en solution injectable, autorisé aux États-Unis, avec des étiquettes uniquement en anglais.
Destinataires
Professionnels de la santé, notamment les hématologues, les oncologues, les infirmiers/-ères en hématologie et en oncologie, et les pharmacien(ne)s.
Messages clés
- Il y a une grave pénurie de PEGASYS (peginterféron alfa-2a) en solution injectable au Canada. Compte tenu des risques graves que cette pénurie présente pour les patients canadiens qui ont été prescrits d’une thérapie à base d’interféron pour le traitement des néoplasmes myéloprolifératifs (NMP), Santé Canada a autorisé FORUS Therapeutics Inc. à importer et à vendre, à titre exceptionnel et temporaire, un produit similaire, mais non identique, le BESREMi (ropeginterféron alfa-2b-njft) en solution injectable, autorisé aux États-Unis, avec des étiquettes uniquement en anglais.
- Au Canada, PEGASYS est indiqué pour le traitement des adultes atteints d’hépatite B et C chronique. Bien que Santé Canada n’ait pas autorisé son usage dans le traitement des NMP, il a été prescrit hors indication pour traiter cette maladie.
- Aux États-Unis, BESREMi est indiqué pour le traitement de la polycythémie vraie (PV), un type de NMP.
- Les professionnels de la santé sont informés des éléments suivants :
- BESREMi contient une substance active différente de celle de PEGASYS et ne doit pas être considéré comme un substitut direct.
- BESREMi possède des indications, des directives posologiques, des considérations d’innocuité et des exigences en matière de surveillance différentes de celles de PEGASYS. Lors de l’évaluation des options thérapeutiques, les professionnels de la santé doivent considérer attentivement ces différences et consulter les renseignements d’ordonnance des États-Unis et les lignes directrices de pratique clinique pertinentes.
- La Food and Drug Administration (FDA) aux États-Unis a approuvé BESREMi en termes d’innocuité et d’efficacité. Toutefois, les patients doivent être informés que BESREMi n’a pas été évalué par Santé Canada en termes d’innocuité, d’efficacité ou de qualité. Face à ce besoin médical critique, Santé Canada a autorisé son importation et sa vente à titre exceptionnel et temporaire.
- Les renseignements d’ordonnance des États-Unis pour BERSEMi, de même que le guide du médicament et son mode d’emploi, disponibles en anglais et en français, contiennent des informations sur l’utilisation du produit en toute sécurité. Il convient de les consulter et de les partager avec les patients, au besoin.
Contexte
Au Canada, PEGASYS est indiqué pour le traitement des adultes atteints d’hépatite B et C chronique. Il a également été utilisé hors indication pour traiter les NMP.
Aux États-Unis, BESREMi est indiqué pour le traitement des adultes atteints de polycythémie vraie (PV), un type de NMP.
Information à l’intention des consommateurs
Au Canada, PEGASYS est approuvé pour le traitement des adultes atteints d’une maladie hépatique chronique causée par le virus de l’hépatite B ou C. Il est également utilisé pour traiter les néoplasmes myéloprolifératifs (NMP), un groupe de cancers du sang caractérisés par une production excessive de cellules sanguines dans la moelle osseuse.
Aux États-Unis, BESREMi est autorisé pour le traitement des adultes atteints de polycythémie vraie (PV), un type de NMP.
En raison d’une pénurie de PEGASYS au Canada, Santé Canada a temporairement autorisé l’importation et la vente de BESREMi, approuvé aux États-Unis. La Food and Drug Administration (FDA) aux États-Unis a approuvé BESREMi en termes d’innocuité et d’efficacité. Toutefois, les patients doivent être informés que BESREMi n’a pas été évalué par Santé Canada en termes d’innocuité, d’efficacité ou de qualité. Face à ce besoin médical critique, Santé Canada a autorisé son importation et sa vente à titre exceptionnel et temporaire. Bien que PEGASYS et BESREMi appartiennent à la même famille de médicaments, BESREMi possède ses propres directives posologiques, considérations d’innocuité et exigences en matière de surveillance.
Les patients à qui BESREMi est prescrit doivent s’adresser à leur professionnel de la santé pour toute question ou préoccupation et suivre ses recommandations pour utiliser le produit. Une surveillance régulière est essentielle au cours du traitement et tout effet indésirable doit être rapidement signalé.
BESREMi est fourni en seringue préremplie contenant 1 ml de solution. Il est possible que les patients doivent jeter une portion de la solution restante dans la seringue afin de respecter leur posologie. Tout médicament excédentaire doit être jeté conformément aux instructions.
Les patients doivent consulter le guide du médicament de BESREMi pour plus d’information et lire attentivement le mode d’emploi avant d’utiliser le produit. Ces deux documents sont disponibles en anglais et en français.
Information à l’intention des professionnels de la santé
PEGASYS et BESREMi sont tous deux des traitements à base d’interféron, mais ce sont des médicaments différents.
Les professionnels de la santé sont informés des éléments suivants :
- BESREMi contient une substance active différente de celle de PEGASYS et ne doit pas être considéré comme un substitut direct.
- BESREMi possède des indications, des directives posologiques, des considérations d’innocuité et des exigences en matière de surveillance différentes de celles de PEGASYS. Lors de l’évaluation des options thérapeutiques, les professionnels de la santé doivent considérer attentivement ces différences et consulter les renseignements d’ordonnance des États-Unis et les lignes directrices de pratique clinique pertinentes.
- La Food and Drug Administration (FDA) aux États-Unis a approuvé BESREMi en termes d’innocuité et d’efficacité. Toutefois, les patients doivent être informés que BESREMi n’a pas été évalué par Santé Canada en termes d’innocuité, d’efficacité ou de qualité. Face à ce besoin médical critique, Santé Canada a autorisé son importation et sa vente à titre exceptionnel et temporaire.
- Les renseignements d’ordonnance des États-Unis pour BERSEMi, de même que le guide du médicament et son mode d’emploi, disponibles en anglais et en français, contiennent des informations sur l’utilisation du produit en toute sécurité. Il convient de les consulter et de les partager avec les patients, au besoin. Consultez les renseignements d’ordonnance des États-Unis pour de l’information sur son usage auprès de populations spécifiques, notamment pendant la grossesse.
Il est également conseillé aux professionnels de la santé d’informer les patients sur les points ci-dessus.
L’étiquetage de BESREMi (voir Annexe 1) est disponible en anglais uniquement et ne comprend pas de texte en français.
BESREMi ne sera pas répertorié dans les logiciels de pharmacie canadiens, les systèmes informatisés de gestion des commandes de produits dans les établissements de santé et les bases de données des régimes d’assurance maladie. Les organisations concernées doivent mettre en place une solution alternative pour assurer la gestion et le suivi des commandes de BESREMi dans ces bases de données.
Par ailleurs, BESREMi ne possède pas de numéro d’identification du médicament (DIN) ni de code-barres compatibles avec les systèmes canadiens de gestion des médicaments. Il est recommandé aux établissements de générer un autocollant personnalisé afin de permettre la lecture du code-barres et d’assurer une identification précise du produit délivré et administré.
Mesures prises par Santé Canada
Afin d’aider à atténuer la pénurie de PEGASYS au Canada, Santé Canada a autorisé FORUS Therapeutics Inc., à titre exceptionnel et temporaire, à importer et à vendre BESREMi, approuvé aux États-Unis. Santé Canada a ajouté ce produit à la Liste des drogues destinées aux importations et aux ventes exceptionnelles.
Santé Canada a collaboré avec FORUS Therapeutics Inc. pour préparer cet avis concernant BESREMi. Santé Canada communique ces renseignements importants en matière d’innocuité aux professionnels de la santé et aux Canadiens par l’entremise de la base de données des rappels et avis de sécurité du site Web Canadiens en santé. La présente communication sera également diffusée par l’entremise du système de notification par courriel MedEffetMC.
Pour signaler un problème lié à la santé ou à l’innocuité
La prise en charge des effets indésirables associés à un produit de santé dépend de leur déclaration par les professionnels de la santé et les consommateurs. Tout effet indésirable grave ou imprévu chez les patients recevant BESREMi devrait être signalé à FORUS Therapeutics Inc. ou à Santé Canada.
FORUS Therapeutics Inc.
200 North Service Road West, bureau 129
Oakville (Ontario) L6M 2Y1
Téléphone : 1-877-359-9595
Télécopieur : 1-877-359-9590
Courriel : forus-pv@innomar-strategies.com
Pour corriger votre adresse postale ou numéro de télécopieur, veuillez communiquer avec FORUS Therapeutics Inc.
Vous pouvez signaler les effets secondaires soupçonnés associés à l’utilisation de produits de santé à Santé Canada :
- Composez sans frais le 1-866-234-2345; ou
- Consultez la page Web de MedEffet Canada sur la Déclaration des effets indésirables (http://www.hc-sc.gc.ca/dhp-mps/medeff/report-declaration/index-fra.php) pour savoir comment faire une déclaration en ligne, par courrier ou par télécopieur.
Pour d’autres renseignements concernant les produits de santé reliés à cette communication, veuillez communiquer avec Santé Canada :
Direction générale de la réglementation des opérations et de l’application de la loi
Courriel : hpce-cpsal@hc-sc.gc.ca
Téléphone : 1-800-267-9675
Originale signée par

Christopher Blowes
Directeur, Affaires réglementaires
FORUS Therapeutics Inc., Oakville (Ontario)
Annexe 1
A. Image du produit BESREMi (ropeginterféron alfa-2b-njft) en solution injectable, autorisé aux États-Unis, boîte et contenu de la boîte
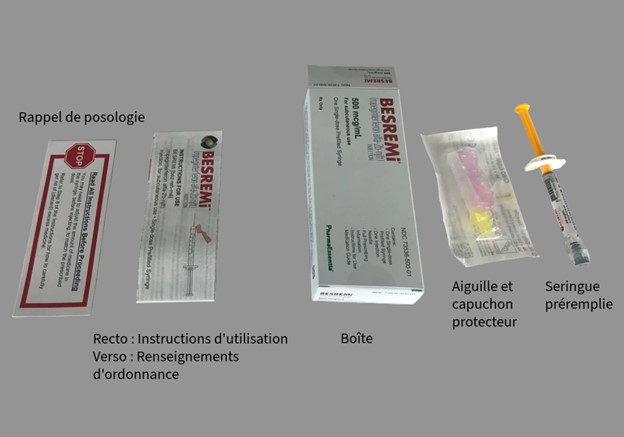
B. Image du produit BESREMi (ropeginterféron alfa-2b-njft) en solution injectable, autorisé aux États-Unis, seringue préremplie à usage unique munie d’une aiguille
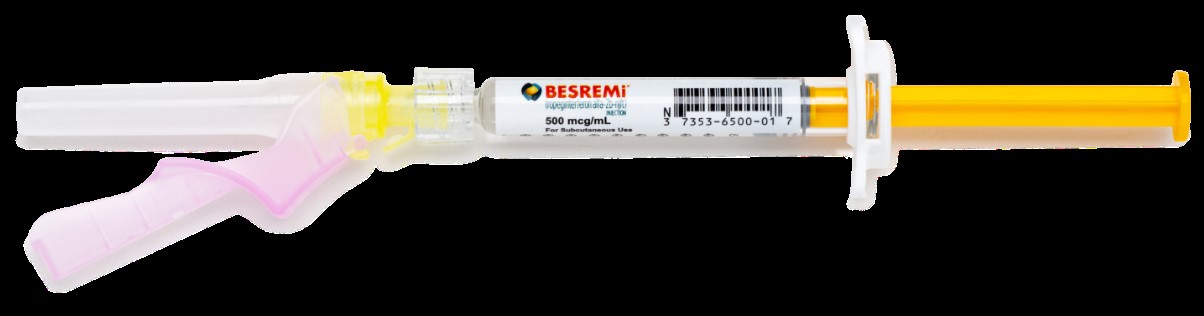
C. Images du produit BESREMi (ropeginterféron alfa-2b-njft) en solution injectable, autorisé aux États-Unis, étiquette de la seringue

D. Images du produit BESREMi (ropeginterféron alfa-2b-njft) en solution injectable, autorisé aux États-Unis, étiquette de la boîte
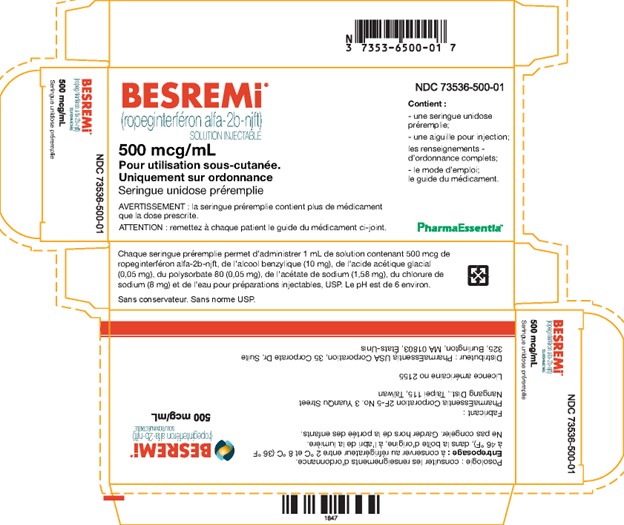
Renseignements supplémentaires
Détails
Recevez des notifications
Recevez des notifications pour les rappels et les avis de sécurité nouveaux et mis à jour, par catégorie.